Проблема необхідності видалення розчиненого кремнію завжди вносила сум’яття в уми продавців систем водопідготовки. Кремній – другий за розповсюдженням в земній корі елемент (поступається тільки кисню). Хімія кремнію за складністю поступається лише хімії вуглецю. Діоксид кремнію (хімічна формула – SiO2) – друга за поширенням у земній корі речовина, яка міститься у різних концентраціях у всіх природних водах. У водопідготовці діоксид кремнію розглядається як забруднююча речовина, здатна відкладати твердий силікатний накип на всіх контактних поверхнях. Відкладення не містять кварц у чистому вигляді, але являють собою силікати, що містять двовалентний або тривалентний катіон.
Тверде з’єднання діоксиду кремнію – кварц. Кварц інертний, але за певних умов (дуже висока температура (> 400оС) та лужне середовище) слабо реагує з водою, утворюючи кремнієву кислоту. Реакція являє собою процес деполімеризації з подальшим гідролізом та утворенням дуже слабких метакремнієвої (силікатної) та ортокремнієвої кислот – відповідно H2SiO3 та H4SiO4. Це пояснює чому діоксид кремнію краще розчиняється в середовищі з високим рН (>10), у присутності великої кількості вільних аніонів ОН–.
Вода з кремнієвою кислотою не може використовуватися для живлення котлів високого тиску через утворення силікатного накипу, що має низьку теплопровідність. Така вода ускладнює роботу котлів та турбін, не придатна для використання у фармацевтиці, текстильній промисловості, інших технологічних процесах, що передбачають нагрівання води до утворення пари або потребують хімічно чистої води. Вимоги до вмісту кремнію у воді для котлів високого тиску – не більше ніж 0,1 мг/л. Відповідно до ДСАНПІН 2.2.4-171-10 вміст кремнію у водопровідній воді не повинен перевищувати 10мг/л.
Водопідготовка. Видалення кремнія.
Колоїдні силікати, які зазвичай представляють незначну частину кремнію в природній воді, видаляються коагуляцією з подальшою фільтрацією. У задачах, що передбачають повне видалення з води кремнію, задіяні в багатоступінчастому поєднанні технології «іонного обміну» та «зворотного осмосу», які дозволяють отримати підсумкові концентрації кремнію у воді не більше 0,1 мг/л.
Зворотній осмос.
Більшість мембран зворотного осмосу мають помірне відторгнення діоксиду кремнію і видаляють кремній ефективніше тільки з підвищенням рН води. Однак у будь-якому випадку системи зворотного осмосу не дозволяють отримати повне видалення з води кремнію.
Іонний обмін.
Всі сильноосновні аніонообмінні смоли (SBA) у гідроксильній формі мають здатність розщеплювати солі. Це означає, що вони мають здатність видаляти слабоіонізовані частинки – CO2 та SiO2. Селективність SBA значно нижча для силікатів ніж для сульфатів і хлоридів, проте значно вище ніж для гідроксиду. При цьому SBA у хлоридній формі має нульову ємність щодо силікатів. Використовуюється тільки гідроксильна форма смоли.
Видалення силікатів іонним обміном – ступінчаста технологія. На першій стадії використовують обробку води сильнокислотним катіонітом у натрієвій формі. На другій стадії – сильноосновний аніоніт у гідроксильній формі (регенерація аніоніту слабким розчином лугу). На другій стадії силікати видаляються разом з іншими аніонами.
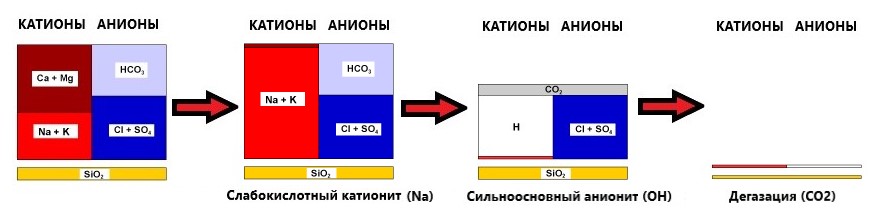
Ця двоступінчаста технологія, подібна процесу “демінералізації”, має масу недоліків, проте, дозволяє видаляти силікати спільно з іншими аніонами. Наостанок варто також відзначити, що традиційна теорія видалення аніонообмінними смолами SiO2 у вигляді іону, наприклад, аналогічно видаленню аніону-бікарбонату, не здатна точно пояснити поведінку SiO2 і труднощі, які виникають з його видаленням.
