Нитрат-селективная ионообменная смола. Снижение содержания нитратов в воде.
Проблема потребления нитратов с питьевой водой.
Около 80% нитратов организм человека получает с пищей и только 20% — с напитками и питьевой водой. Существует прямая коррелляция между потреблением нитратов и раком желудочно-кишечного тракта у взрослых и метагемоглобинемией у детей. Превышение допустимого уровня нитратов в грунтовой воде – красный флажек для владельца домохозяйства. Нужно проявить осторожность – нитраты могут указывать на присутствие в воде других загрязнений из перечисленных источников. Источники нитратов в воде – сельскохозяйственные удобрения и животноводческие фермы, открытые септики, свалки отходов, разложение растительности.
Природное содержание в грунтовой воде нитратов в редких случаях превышает 1 мг N/л (NO3-N). Поэтому любое значение выше 3 мгN/л уже указывает на антропогенное происхождение.
Поглощенные нитраты поддерживают выработку оксида азота в организме, который улучшает кровоток и снижает артериальное давление. Однако оксид азота окисляется до нитритов, которые и являются настоящими возмутителями спокойствия. Нитриты реагируют с гемоглобином, образуя метагемоглобин, который является плохим переносчиком кислорода в крови.
Для взрослых длительное воздействие высоких уровней нитратов представляет канцерогенную опасность, увеличивая риск рака толстой кишки, почек и желудка. Нитраты также могут реагировать с аминами и амидами, образуя нитрозосоединения, также известные как канцерогенные.
Согласно Европейским рекомендациям по безопасности пищевых продуктов 2017 года, допустимое количество нитрита в день составляет около 0,06 миллиграмма на 1 килограмм веса взрослого человека. Для среднего человека весом 70 кг это составляет 4,2 мг нитрита в день. Вяленый бекон содержит около 120 мг нитритов в киллограме! В 2015 году ВОЗ классифицировала переработанное мясо как канцерогенное, если оно содержало добавленные нитраты. Это помещает переработанное мясо в ту же категорию риска, что и курение табака или воздействие асбеста.
Какой уровень нитратов в питьевой воде можно считать безопасным?
В настоящее время EPA (Агентства по охране окружающей среды США) установило безопасное значение нитратов на уровне 10 мгN/л (азот нитратный NO3-N) и нитритов – 1 мгN/л (азот нитритный NO2-N). ВОЗ поддерживает аналогичные рекомендации. Эти уровни измеряют только содержание азота в ионе и не отражают общий ионный уровень нитрата или нитрита. Соответственно, 10 мгN/л азота нитратного = 44,3 мг/л нитрат-иона (NO3) или 35,7 мг/л в пересчете на CaCO3 и 1 мгN/л азота нитритного = 3,3 мг/л нитрит-иона (NO2) или 3,6 мг/л в пересчете на CaCO3. Эти значения соответствуют MCL (maximum contamination level, ПДК для муниципальной питьевой воды). При этом MCLG (maximum contamination level goal, целевая концентрация примеси, на которую должно ориентироваться значение MCL, если есть такая возможность) = MCL.
Многочисленные национальные и международные исследования указывают на повышенные канцерогенного риска при потреблении воды с содержанием азота нитратного более 0,14 мгN/л (0,6 мг/л по NO3). Это означает, что употребление воды с нитратами ниже национальных и международных ПДК может по прежнему представлять опасность. Муниципальные водоканалы будут поддерживать уровень нитратов ниже норматива, поставляя законно приемлемый продукт. Поддержание законного уровня нитратов предполагает смешивание проблемной воды с водой из источника с низким уровнем нитратов. Это представляется законным технологическим решением, но не полезным для здоровья человека. В США Бюро переписи населения показало за 2007 год, что водоснабжение более 15 млн домохозяйств осуществлялось из частных скважин, вода в 10% из которых содержала азот нитратный в концентрации более 10 мгN/л. ПДК примесей в воде в частных скважинах не контролируется, однако потребители этой воды не освобождаются от последствий. Как минимум, на сегодняшний день в Украине ситуация ничем не лучше.
Почему национальные и международные ПДК не поддерживают безопасный уровень?
Ответ простой – цена. Как Вы думаете, какое количество средств нужно инвестировать в муниципальные водоканалы для построения заводов по снижению уровня нитратов? Возможно это объясняет почему EPA и ВОЗ выбрали другой взгляд на ситуацию.
Однако, то, что не могут обеспечить муниципальные водоканалы открывает возможности для квалифицированных поставщиков водоочистного оборудования, предоставляя большой рынок для новых систем водоподготовки.
Какую из технологий удаления нитратов в водоподготовке можно рассматривать как Наилучшую Доступную Технологию?
Обратный осмос способен сохранять эффективность удаления нитратов на уровне до 90%. Однако, для достижения приемлемого результата обратный осмос производит слишком много отходов и требует слишком много энергии (на поддержание высокого давления на мембрану) если рассматривать любой вариант централизованой водоподготовки. Наиболее еффективная и простая технология – это ионный обмен.
Эта технология способна снизить нитраты практически до неопределяемого уровня (более 95%) и использовать полученную воду для подмеса к воде из скважин с содержанием нитратов выше нормативного уровня. Нитратные системы основаны на применении сильноосновной анионообменной смолы, регенерируемой раствором NaCl точно так же как и обычные системы умягчения. За исключением применяемой смолы нитратные системы конструктивно аналогичны системам умягчения.
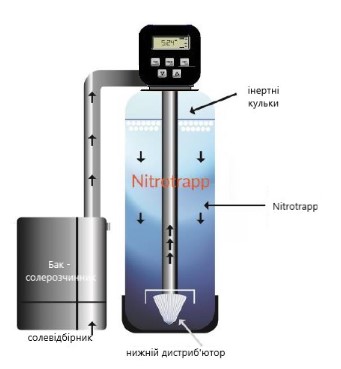 Эта технология также предпочтительна для бытовой подготовки воды «на входе в дом». Ионный обмен сохраняет компактность и расходует на регенерацию незначительное количество воды — 2..3%. Бытовые нитратные ионообменные системы представлены разными типоразмерами с автоматической работой и регенерацией. При использовании правильно подобранной смолы такие системы способны также удалять другие анионные примеси, содержащие в составе уран, хром, селен или мышьяк.
Эта технология также предпочтительна для бытовой подготовки воды «на входе в дом». Ионный обмен сохраняет компактность и расходует на регенерацию незначительное количество воды — 2..3%. Бытовые нитратные ионообменные системы представлены разными типоразмерами с автоматической работой и регенерацией. При использовании правильно подобранной смолы такие системы способны также удалять другие анионные примеси, содержащие в составе уран, хром, селен или мышьяк.
Существует два обобщенных класса сильноосновных анионообменных смол для удаления нитратов: нитратселективная смола и стандартная неселективная смола. Обе смолы имеют собественные области применения.

Как выбрать смолу? Анализируем концентрации нитратов и сульфатов.
Стандартная сильноосновная анионообменная смола гелевого типа не относится к нитратселективным смолам. Эта смола будет равноценно обменивать хлориды как на нитраты, так и на сульфаты. Однако, есть ньюанс – по мере приближения к истощению обменной емкости смола сначала будет вытеснять в воду нитраты, заменяя их сульфатами. Это создаст проблему — в определенный период времени обработанная вода будет содержать нитратов больше чем питающая вода. Это явление получило название «сброса» или «вытеснения». Сброс предполагает, что в обработанную воду может вытесняться из смолы концентрация нитратов, равная сумме концентрации нитратов и сульфатов в исходной воде. Для примера, если исходная вода содержала 80 мг/л нитратов и 85 мг/л сульфатов в процессе истощения емкости смолы появляется проскок в обработанную воду нитратов, который продолжает расти вплоть до значения 165 мг/л. Фактически пиковая концентрации нитратов зависит от общей и относительной концентрации всех ионов в исходной воде. Разумно предположить наихудший вариант развития, особенно для небольших бытовых систем, которые не имеют средств мониторинга нитратов в обработанной воде.
Стандартная сильноосновная анионообменная смола будет создавать меньший проскок и поддерживать большую обменную емкость если питающая вода содержит нитраты и сульфаты в соотношении 2:1 и выше. В дополнение существует правило недооценивать обменную емкость нитратных систем вплоть до 50% в условиях если состав воды не отличается стабильностью. Если уровень нитратов в несколько раз превышает ПДК можно также установить два модуля последовательно, чтобы гарантировано избежать последствий сброса нитратов.
Нитрат-селективная анионообменная смола также обменивает как нитраты, так и сульфаты. Однако, в процесее истощения емкости такая смола сначала вытесняет сульфаты. Нитрат-селективная смола – лучший выбор, если в исходной воде концентрация сульфатов преобладает над концентрацией нитратов. Концентрация сульфатов всегда оказывает влияние как на обменную емкость нитратной системы, так и на проскок нитратов. В исходной воде с очень высоким общим солесодержанием проскок нитратов может превышать ПДК (MCL), что подразумевает необходимость установки последовательно второго модуля с уменьшением обменной емкости первого модуля на 30%.
Сильноосновные аниониты имеют гораздо более высокую селективность к нитратам, чем к нитритам.
Химия анионов.
Анионообменные смолы характеризуются положительным зарядом и улавливают отрицательно заряженные ионы – анионы. Большинство матриц анионообменных смол изготовлены из стирола, сшитого дивинилбензолом. Для обеспечения функциональности смолы обрабатываются промежуточными соединениями, аминосоединениями и заканчиваются обменными хлоридами.
В США для удаления нитратов ионным обменом наиболее часто применяют стандартные неселективные сильносновные аниониты типа I и типа II. Функциональные группы гелевых анионитов типа I – триметиламины, типа II – диметиламины с более слабым зарядом. Более слабый заряд облегчает регенерацию и предоставляет большую емкость для заданного уровня регенеранта.
Функциональные группы нитрат-селективных смол – триметиламины или трипропиламины. Большая аминогруппа создает помеху для большой молекулы сульфата, поддерживая более слабую связь. Это тот момент, который делает эту смолу «сульфат-деселективной» и «нитрат-селективной». Также существуют супер-нитрат-селективные смолы на основе функциональной группы из трибутиламина. Однако такая «супер-селективность» смолы в отношении нитрата крайне затрудняет процесс регенерации раствором хлорида натрия (NaCl).
Гелевый анионит типа II — это рабочая лошадка для удаления нитратов, который часто выбирают муниципалитеты для обработки воды с высоким уровнем нитратов и низким уровнем сульфатов. Железо должно быть предварительно удалено из воды. Если анионит типа II регенерируется солью и жесткость исходной воды больше 5 мг-екв/л возможно преобразование гидрокарбонатов в нерастворимые карбонаты с последующим процессом цементации смолы карбонатами. В таком случае регенерирующий раствор в процессе регенерации подкисляют лимонной кислотой для предотвращения карбонатного обрастания смолы. Также рекомендуется регенерировать анионообменную гелевую смолу умягченной водой. Аниониты типа II несколько дороже анионитов типа I. К положительным свойствам анионитов типа I можно отнести тенденцию к меньшему сбрасу нитратов по мере истощения смолы.
Конструкция нитратной системы.
Для обработки воды с высоким или неизвестным содержанием сульфатов нитрат-селективные смолы – наиболее безопасный выбор. Нитрат-селективные смолы с функциональными группами из триметиламинов (TEA) или трипропиламинов (TPA) характеризуются большой обменной емкостью в присутствии сульфатов и предотвращают сброс нитратов при истощении смолы. Эти смолы дороже неселективных анионитов типа II. Супер-селективные смолы демонстрируют самую высокую селективность к нитратам и полное отсутствие сброса нитратов при истощении. Однако, для регенерации таких смол, обладающих очень высокой селективностью к нитратам, потребуется соли (NaCl) в 3-4 раза больше в сравнении с обычной нитрат-селективной смолой.
| Характеристики | Муниципальные нитратные системы | Бытовые нитратные системы |
| Линейная скорость | 25 м/ч | 35 м/ч |
| Объемная скорость | 8…40 BV/ч | 8…40 BV/ч |
| Глубина слоя (co-flow) | 1500 мм min | 900 мм min |
| Глубина слоя (counter-flow) | 1800 мм min | 1200 мм min |
| Срок службы смолы | ~ 10 лет | ~ 5-7 лет |
